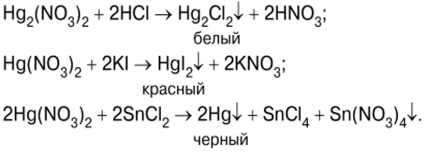
Imoibrithe comhdhúile mearcair
Tá mearcair miotalach agus a chomhdhúile an-tocsaineach d'orgánaigh bheo. Tá sé seo fíor go háirithe maidir le comhdhúile atá an-intuaslagtha in uisce. Ba chóir a bheith an-chúramach agus tú ag tástáil le teaglaim den eilimint uathúil seo (is é mearcair an t-aon mhiotal atá leacht ag teocht an tseomra). Cloí le bunorduithe poitigéara? ligfidh tú chun roinnt turgnaimh a dhéanamh go sábháilte le comhdhúile mearcair.
Sa chéad turgnamh faighimid amalgam alúmanaim (tuaslagán den mhiotal seo i mearcair leachtach). Tuaslagán mearcair (II) Hg níotráite (V) Hg (UIMH3)2 agus píosa sreang alúmanaim (grianghraf 1). Cuirtear slat alúmanaim (glantar go cúramach de thaiscí) i bhfeadán tástála le tuaslagán de salann mearcair intuaslagtha (grianghraf 2). Tar éis roinnt ama, is féidir linn scaoileadh boilgeoga gáis a urramú ó dhromchla na sreinge (grianghraif 3 agus 4). Tar éis an slat a bhaint as an réiteach, tharlaíonn sé go bhfuil an cré clúdaithe le sciath fluffy, agus ina theannta sin, feicimid freisin liathróidí mearcair mhiotalacha (grianghraif 5 agus 6).
Ceimic - taithí ar mhearcair a chomhcheangal
Faoi ghnáthchoinníollacha, tá dromchla an alúmanam clúdaithe le ciseal dlúth ocsaíd alúmanaim.2O3leithlisíonn sé miotail go héifeachtach ó thionchair ionsaitheacha comhshaoil. Tar éis an slat a ghlanadh agus a thumadh i dtuaslagán de shalann mearcair, díláithrítear ions Hg2+ alúmanam níos gníomhaí:
Déanann mearcair a thaisctear ar dhromchla an tslat cónascadh le alúmanam, rud a fhágann go mbíonn sé deacair don ocsaíd cloí leis. Is miotail an-ghníomhach é alúmanam (imoibríonn sé le huisce chun hidrigin a scaoileadh - breathnaítear boilgeoga gáis), agus is féidir é a úsáid mar ábhar struchtúrach mar gheall ar a dhlúth ocsaíd ocsaíd.
Sa dara turgnamh braithfidh muid iain NH amóiniam.4+ ag baint úsáide as imoibrí Nessler (b é an poitigéir Gearmánach Julius Nessler an chéad duine a d’úsáid in anailís é sa bhliain 1856).
Déan turgnamh ar imoibriú leannlusanna agus comhdhúile mearcair
Tosaíonn an tástáil le deascadh mearcair(II) iaidíde HgI.2, tar éis tuaslagáin d'iaidíd photaisiam KI agus mearcair (II) níotráit (V) Hg (NO3)2 (grianghraf 7):
deascán oráiste-dearg HgI2 (grianghraf 8) ansin déan cóireáil le farasbarr de thuaslagán iaidíde potaisiam go dtí go bhfaightear comhdhúil choimpléascach intuaslagtha de fhoirmle K2HgI4 ? Tetraiodercurate Potaisiam(II) (Grianghraf 9), ar imoibrí Nessler é:
Ag baint úsáide as an gcomhdhúil mar thoradh air is féidir linn iain amóiniam a bhrath. Beidh tuaslagáin de hiodrocsaíd sóidiam NaOH agus clóiríd amóiniam NH fós ag teastáil.4Cl (grianghraf 10). Tar éis méid beag de thuaslagán salann amóiniam a chur leis an imoibrí Nessler agus an meán a alcalú le bonn láidir, breathnaimid ar fhoirmiú dath buí-oráiste in ábhar an fheadáin tástála. Is féidir an t-imoibriú reatha a scríobh mar:
Tá struchtúr casta ag an gcomhdhúil mearcair mar thoradh air:
Úsáidtear tástáil an-íogair Nessler chun fiú rianta de shalainn amóiniam nó amóinia in uisce (amhail uisce sconna) a bhrath.

